生活節奏緊湊,「身體已經極度疲憊,躺在床上大腦卻停不下來」已成為許多人的夜間常態 。這種現象往往不是單純的睡不好,而是持續性壓力導致的睡眠節律混亂 。長期高壓下,自律神經系統維持在高度警戒,導致交感神經在夜間過度活化,干擾深層睡眠並造成頻繁夜醒 。長期高壓下,自律神經系統維持在高度警戒,導致交感神經在夜間過度活化,干擾深層睡眠並造成頻繁夜醒 。
相關研究指出:睡眠、壓力與腸道菌相之間存在雙向關係:睡眠受損會影響腸道與免疫,而腸道菌相失衡也會回頭干擾睡眠與情緒,形成惡性循環 。
對於經常受壓力型失眠所苦的族群而言,理解壓力與睡眠之間的雙向關係是改善的關鍵。若忽視壓力訊號,不僅會讓睡眠品質持續惡化,更可能引發其他生理系統的失衡,讓身體陷入難以掙脫的惡性循環。
一、深入了解:壓力型失眠是什麼?
壓力型失眠主要描述因心理壓力、焦慮或急性生活事件引發的睡眠障礙 。
- 過度警覺理論 (Hyperarousal Theory):這類失眠的核心機制在於大腦警覺系統無法在夜間降低,導致神經系統持續釋放壓力荷爾蒙,使人在入睡時仍保持高度環境監測與認知活躍 。
- 認知反芻 (Rumination):不同於生理性失眠,壓力型失眠者常在睡前過度擔憂睡眠本身,產生「預期性焦慮」,進一步推升自律神經活躍度。
- 辨識壓力型失眠的常見跡象-入睡困難:躺在床上超過 30 分鐘仍無法入睡,腦袋不斷思考。
- 睡眠維持困難:半夜反覆驚醒,醒後大腦瞬間清醒,難以再入眠 。交感神經亢奮反應:睡前伴隨肌肉緊繃、淺呼吸或腸胃不適 。對睡眠的預期性焦慮:看著時鐘感到壓力,擔心隔天精神不濟 。
- 凌晨易驚醒:提早醒來並開始思考工作代辦事項,難以再睡回去。
二、HPA 軸:壓力反應系統是什麼?為什麼會讓人越累越清醒?
HPA 軸的正式名稱為「下視丘-腦垂體-腎上腺軸」,(Hypothalamic-Pituitary-Adrenal axis,簡稱 HPA 軸),HPA 軸是人體主要的壓力應對系統。當大腦偵測到威脅或壓力時,下視丘會啟動信號,促使腎上腺皮質分泌「皮質醇」(Cortisol),也就是壓力荷爾蒙。
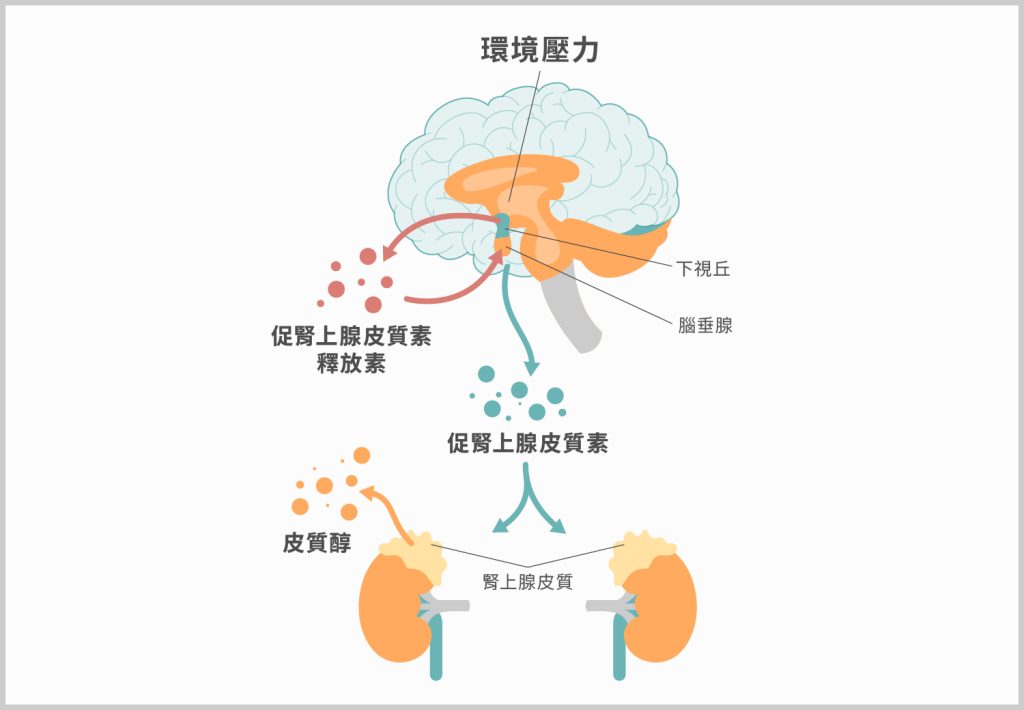
圖一、下視丘-腦垂體-腎上腺軸
皮質醇節律失調的影響
為什麼高壓環境會導致越累越清醒?在正常生理狀態下,皮質醇的濃度會遵循日夜節律:皮質醇應在早晨達到高峰喚醒身體,傍晚下降幫助大腦放鬆,準備入睡 。早當面臨長期的工作壓力、情緒焦慮或生活劇變的高壓狀況下,大腦會誤判身體持續處於危險之中,導致 HPA 軸過度活躍,皮質醇無法在夜間正常降低,會抑制褪黑激素生成並維持交感神經亢奮,導致大腦無法停止運轉 。
| 生理狀態 | 早晨皮質醇表現 | 夜間皮質醇表現 | 睡眠與精神狀態 |
| 正常節律 | 濃度達高峰 | 濃度逐漸降至最低 | 早晨精神飽滿,夜間順利產生睡意並入睡 |
| 慢性壓力失調 | 濃度提前達高峰 | 濃度異常偏高 | 早晨容易提早驚醒,夜間思緒活躍、難以入眠 |
表一、皮質醇節律對身體的影響對照表
三、腸腦軸:慢性壓力如何改變腸道與發炎反應?陷入惡性循環
人體的壓力反應不僅侷限於大腦與內分泌系統,更會直接衝擊消化道環境。科學研究證實,消化道與大腦間有密切的雙向溝通管道(腸腦軸)。當 HPA 軸因壓力過度活化,會改變腸道黏膜通透性與菌叢平衡 。
壓力如何引發「腸漏現象」、全身發炎與干擾神經系統
- 菌叢失衡:體內益菌減少,致病菌增加 。這種微生態失衡(Dysbiosis)會削弱腸道黏膜的防禦能力。
- 腸漏現象 (Leaky Gut):腸壁細胞間隙鬆脫,細菌毒素(如 LPS)滲入。腸道屏障受損,原本應該被阻擋在腸道內的細菌毒素與未消化的大分子,便有機會滲入血液循環中,引發全身性的免疫發炎反應。
- 神經發炎:促發炎細胞激素(Cytokines)穿過血腦屏障,干擾睡眠調節中樞與血清素合成路徑。
根據臨床觀察,慢性壓力與失眠患者的血液樣本中,特定的促發炎細胞激素(Cytokines)常呈現異常升高趨勢。這些發炎因子會:
- 穿過血腦屏障,影響中樞神經系統:干擾睡眠調節中樞的運作,進一步刺激 HPA 軸,讓身體承受更大的壓力,形成難以打破的惡性循環。
- 干擾血清素與褪黑激素的合成路徑:進一步惡化睡眠品質。
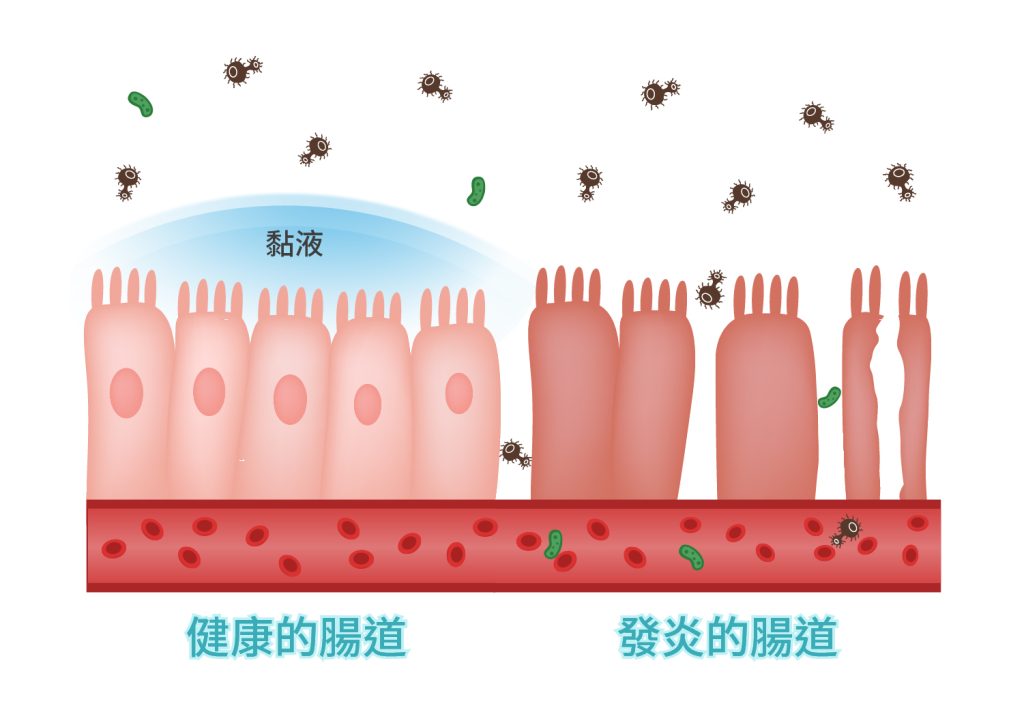
圖二、腸道屏障受損導致腸漏
以下列出步驟說明慢性壓力引發腸腦發炎循環的機制:
步驟1、壓力荷爾蒙干擾:大腦感知慢性壓力,持續釋放過量皮質醇,改變腸胃蠕動與胃酸分泌。
步驟2、腸道微生態失衡與屏障受損:腸道好菌減少,黏膜防禦力下降,引發腸漏現象。
步驟3、內毒素滲透與全身發炎:腸道內的細菌內毒素(如 LPS)進入血液,免疫系統啟動,釋放發炎因子。
步驟4、神經性發炎加劇失眠:發炎因子影響大腦,降低血清素合成並刺激神經元,導致焦慮加重與睡眠結構破碎。
下表整理出壓力影響下,腸道菌群與發炎指標的具體變化數據:
| 類別 | 觀測指標 | 壓力下的變化趨勢與文獻數據 |
| 促發炎指標 | C-反應蛋白 (CRP) | 睡眠片段化者濃度平均高出約 25% |
| 白血球介素-6 (IL-6) | 慢性失眠者夜間分泌量顯著增加,與日間疲勞感正相關 | |
| 腸道益菌 | 雙歧桿菌 (Bifidobacterium) | 處於高壓力環境下,受試者體內的雙歧桿菌豐度平均下降約 30–50% |
| 乳酸桿菌 (Lactobacillus) | 慢性應激症會顯著抑制乳酸桿菌的生長,減少維持腸道屏障的功能 |
表二、壓力下的腸道菌群與發炎觀測指標變化
四、壓力型失眠的睡眠片段化:為什麼睡再久都還是累?
壓力型失眠最痛苦的是「睡眠被切碎」,稱為睡眠片段化 (Sleep Fragmentation) 。這會導致身體無法進入「慢波深層睡眠」與「快速動眼期 (REM)」,使身體修復感下降 。
睡眠效率 (Sleep Efficiency, SE) 的臨床指標
當壓力系統持續活化,大腦會處於一種低度的警覺狀態,導致睡眠深層不足,容易在淺層睡眠階段(第一、二期)因微小的干擾而驚醒。
這種被切碎的睡眠結構,會讓身體無法順利進入修復功能最核心的「慢波深層睡眠」(Slow-wave Sleep)與記憶整合的「快速動眼期」(REM Sleep)。即使總睡眠時數看起來足夠,但由於缺乏結構完整的睡眠週期,醒來後依然會感到大腦昏沈、肌肉疲憊,且情緒調節能力下降。
睡眠效率(Sleep Efficiency, SE)是衡量睡眠品質的硬指標(實際入睡時間 / 躺床總時間)。當其數值下降時,大腦的認知運作與神經傳導會出現顯著受損。
| 睡眠效率 (SE) | 臨床定義標準 | 認知與生理損害表現 |
| 85% 以上 | 正常範圍 | 神經修復正常,專注力與記憶鞏固功能良好。 |
| 80% – 84% | 輕度受損 | 警覺性下降,偶爾短暫分心,決策反應時間平均延遲約 10% 。 |
| 75% – 79% | 中度受損 | 工作記憶容量顯著縮減,情緒波動增加,出錯率較正常者高出約 1.5 倍。 |
| 75% 以下 | 嚴重失調 | 執行功能大幅衰退,邏輯推理與資訊處理速度顯著變慢。 |
表三、睡眠效率與生理損害表現
為什麼睡眠失調比睡得少更嚴重?
壓力型失眠者常出現「不安穩的 REM」,導致大腦無法剝離記憶中的負面情緒,使得隔天焦慮感持續累積 。
正常的睡眠由數個 90 分鐘的週期組成,每個週期包含從淺入深再到REM做夢的過程。壓力型失眠者往往在進入深層睡眠前就發生「微覺醒」(Micro-arousals),打斷身體分泌生長激素與清除大腦代謝廢物(如類澱粉胜肽)的黃金時間。
| 比較項目 | 正常睡眠結構 | 壓力型失眠結構 |
| 入睡潛伏期 | 通常在 20 分鐘內入睡 | 往往超過 30 分鐘,且伴隨反芻思考 |
| 深層睡眠比例 | 佔總睡眠約 15–25% | 比例顯著下降,身體修復感差 |
| 覺醒次數 | 夜間覺醒次數少於 1 次 | 頻繁覺醒>3 次,且醒後難再入睡 |
| 醒後感受 | 神清氣爽、情緒穩定 | 焦慮感重、注意力不集中、易怒 |
表四、正常睡眠與壓力型睡眠的結構差異
破碎的 REM 睡眠與情緒記憶處理
快速動眼期(REM)是大腦處理情緒與重整記憶的關鍵階段。壓力型失眠者常出現「不安穩的 REM」(Restless REM),即雖然進入做夢期,但因交感神經活性過高,導致該階段被頻繁切斷。
當 REM 睡眠比例異常或品質不佳時,大腦將失去「解耦聯」(Decoupling)的能力。正常情況下,大腦會在睡夢中剝離記憶中的負面情緒色彩,但壓力型失眠者的 REM 片段化,會導致前一天的壓力和焦慮情緒無法被稀釋,使得負面記憶在隔天依然鮮明,這也是壓力感持續累積、難以消除的核心原因。
以下列出睡眠結構崩解的惡性循環:
- 警覺門檻降低:HPA 軸活化使大腦對聲音、光線過度敏感,誘發頻繁微覺醒。
- 深層睡眠不足:身體修復感消失,大腦毒素無法清除,早晨起床伴隨明顯的肌肉僵硬或疲累。
- 情緒處理失效:碎片化的 REM 讓情緒壓力無法代謝,加劇隔天的焦慮感。
- 日間代償行為:頻繁補眠或過度攝取咖啡因等提神物質,進一步破壞次晚的睡眠結構。
五、關鍵修復:腸道菌如何調節睡眠節律?
許多人認為睡眠僅是大腦的責任,但科學研究證實,腸道微生態(Gut Microbiota)在維持睡眠節律中扮演關鍵角色。腸道被稱為「人類的第二個大腦」,透過神經、內分泌與免疫系統與中樞神經進行雙向溝通,即為「腸腦軸」(Gut-Brain Axis)。腸道菌不僅協助消化,更能合成影響情緒與睡眠的多種神經傳導物質。
腸道菌影響睡眠的四種關鍵生化路徑
- 血清素與褪黑激素路徑,關鍵前驅物生成:人體 90% 以上的血清素(Serotonin)在腸道合成,不僅能調節情緒,也是晚上大腦是合成褪黑激素的原料(Melatonin)。特定的腸道菌(如某些乳酸桿菌與雙歧桿菌)能協助分解色胺酸(Tryptophan),這是合成血清素的重要前驅物,若腸道合成功能不佳,將導致正常入睡節律所需的褪黑激素不足。
- 營養素轉化與神經傳導物質的直接生成:部分腸道微生物具備生成 GABA(γ-胺基丁酸)的能力。GABA 是人體內最重要的抑制性神經傳導物質,負責降低神經元的興奮度、緩解焦慮並啟動睡眠。研究顯示,腸道內益菌所產生特定的短鏈脂肪酸(Short-chain Fatty Acids, SCFAs)亦能調控中樞神經系統內的 GABA 受體活性。
- 迷走神經的快速通訊:迷走神經(Vagus Nerve)有如腸腦軸的「高速公路」。腸道菌產生的代謝產物能刺激迷走神經末梢,將生理壓力或放鬆訊號在毫秒間傳達至大腦的孤束核(Nucleus of the Solitary Tract, NTS),進而影響日間的警覺性與夜間的睡眠深度。
- 調控HPA軸,睡眠節律啟動:腸道菌群能調節,調降皮質醇分泌,並將血清素轉化為褪黑激素,誘導深度睡眠。
六、從腸道調整睡眠節律:精神益生菌可以扮演什麼角色?
在腸腦軸研究的進程中,「精神益生菌」(Psychobiotics)的發現為壓力型失眠提供了新的調節策略。精神益生菌是指攝取適量後,能透過菌腸腦軸與中樞神經互動,對宿主精神心理健康產生正面影響的活體微生物。
精神益生菌如何改善壓力型失眠?
研究顯示,這類特定菌株與普通益生菌的不同之處在於,它們具有調節神經傳導物質或抑制 HPA 軸過度活化的能力。透過腸腦軸給予訊號,協助大腦從「戰或逃」的警戒模式切換至「放鬆與修復」模式,從根本上優化睡眠結構。
精神益生菌並非像安眠藥般直接強迫大腦進入睡眠,而是透過降低血液中的皮質醇濃度,以及提升體內 GABA 或血清素的自然合成,來創造一個更有利於入睡的生理環境。
以下為特定益生菌菌株經實證與睡眠及壓力調節相關:
- 植物乳桿菌 PS128:研究指出能有效降低皮質醇濃度,調節腦中多巴胺與血清素代謝,協助降低高壓族群的入睡潛伏期,提升睡眠效率(Sleep Efficiency)並增加深層睡眠時間。
- 發酵乳桿菌PS150:研究指出在改善中度失眠與生理時鐘失調方面展現了顯著效益,能提升褪黑激素(Melatonin)濃度、優化日間食慾素(Orexin)調節並重塑晝夜節律(Circadian Rhythm)。
- 瑞士乳桿菌 Rosell-52:常與長雙歧桿菌聯用,文獻顯示可降低夜間皮質醇分泌。
- 短雙歧桿菌 CCFM1025:透過腸腦軸調節慢性壓力反應,幫助產生GABA,具備提升深層睡眠比例的潛力。
從腸道生態調節睡眠是一項長期的生理過程,不同於安眠藥僅幫助入睡,卻沒有改善壓力型失眠與睡眠結構的功能。以下列出透過腸道從源頭改善睡眠節律的方法:
- 評估與篩選特定菌株:優先挑選具有臨床文獻支持、針對能夠降低壓力、調節睡眠結構的特定精神益生菌株,並確認產品的菌株編號。
- 穩定補足益生元原料:選擇含有益生質的精神益生菌產品。每日飲食中需包含足夠的膳食纖維,為益生菌提供生長所需的能量來源,強化菌叢在腸道內的定殖時間。
- 維持習慣持續性補充:腸道菌相的改變平均需要 4 至 8 週的時間。在此期間需維持規律攝取,把維持腸道環境健康與補充精神益生菌當作長期調養的方式,讓身體養成自然完整的睡眠節律。
- 結合睡眠衛生與節律調整:在調整腸道微生態的同時,嘗試調整睡眠習慣,睡前 1 小時減少藍光刺激,利用腸腦軸的天然放鬆訊號,加速褪黑激素、血清素與GABA的自然分泌。
對於不想依賴藥物、或正在尋找輔助調節方式的人來說,精神益生菌提供了一個有科學根據的選擇。強調長期平衡與系統性調節,不僅限於「讓人睡著」,而在於從壓力、情緒與睡眠節律之間整體調節改善,協助身體逐步找回更穩定的睡眠狀態。
FAQ
1. 壓力型失眠和一般睡不好有什麼不同?
核心差異在於大腦的「過度警覺」。一般失眠常由環境或生理不適引起,而壓力型失眠是大腦警覺系統無法降載,神經持續釋放皮質醇,導致對睡眠產生預期性焦慮,陷入越想睡越清醒的生理困境。
2. 為什麼明明很累,晚上反而更清醒?
這是壓力反應系統(HPA軸)失調所致。長期壓力使皮質醇在夜間異常偏高,直接抑制褪黑激素生成並維持交感神經亢奮。這讓身體雖感到肉體疲倦,大腦卻如同處於備戰狀態般無法停止運轉。
3. 壓力為什麼會影響腸道,甚至讓睡眠更糟?
壓力經由「菌-腸-腦軸」減少益生菌並削弱腸道黏膜,引發發炎反應。這些發炎因子會干擾中樞神經,破壞睡眠調節機制。受損的腸道功能與失眠相互加劇,形成壓力、腸道發炎與睡眠障礙的惡性循環。
4. 壓力型失眠最麻煩的地方是什麼?
最核心困境是「睡眠片段化」。大腦持續處於低度警覺,導致睡眠結構被切碎,難以進入深層修復期與快速動眼期(REM)。這會大幅降低睡眠效率,使人醒後依舊昏沈,隔日對壓力的耐受度進一步下降。
5. 腸道菌怎麼影響睡眠?
腸道菌透過「腸腦軸」影響睡眠:高達95%血清素在腸道合成,是製造褪黑激素的關鍵原料。特定好菌能分泌GABA緩解焦慮,並經由迷走神經向大腦發送放鬆訊號,抑制壓力系統,從根源優化睡眠結構並加深睡眠深度。
6. 精神益生菌與安眠藥有什麼不同?
安眠藥與精神益生菌的運作原理完全不同:
安眠藥屬中樞神經抑制劑,強迫進入淺眠卻難以深層修復。精神益生菌則透過「腸腦軸」調節血清素與 GABA,抑制 HPA 軸壓力系統。它非即時鎮靜,而是優化腸道生態與睡眠結構,讓大腦從警戒轉向自然放鬆,找回深層睡眠。
參考資料
- Palagini, L., et al. (2022). Sleep Deprivation and Insomnia in Adolescence: Implications for Mental Health. Children, 10(5).
- Riemann, D., et al. (2022). Insomnia disorder: State of the art and future vicissitudes. Journal of Sleep Research, 31(6).
- Riemann, D., et al. (2020). The hyperarousal model of insomnia: A review of the concept and its evidence. Sleep Medicine Reviews, 52.
- Fernandez-Mendoza, J. (2021). The cognitive and physiological hyperarousal model of insomnia. Current Psychiatry Reports, 23(12).
- Spencer, R. L., et al. (2022). The hypothalamic-pituitary-adrenal axis in stress and health. Endocrine Reviews, 43(1).
- Nicolaides, N. C., et al. (2021). Stress, the stress system and the role of glucocorticoids. Neuroimmunomodulation, 28(1).
- De Nys L, Anderson K, et al. The effects of physical activity on cortisol and sleep: A systematic review and meta-analysis. Psychoneuroendocrinology. 2022 Sep;143:105843.
- Bush, B., & Hudson, T. (2021). The Role of Cortisol in Sleep. Integrative Medicine: A Clinician’s Journal, 20(2).
- Mayer, E. A., et al. (2022). The microbiome-gut-brain axis in health and disease. Nature Reviews Gastroenterology & Hepatology, 19(1).
- Madison, A., & Kiecolt-Glaser, J. K. (2021). Stress, depression, diet, and the gut microbiota: human-bacteria interactions at the core of psychoneuroimmunology and nutrition. Current Opinion in Behavioral Sciences, 28.
- Irwin MR, Olmstead R, Carroll JE. Sleep Disturbance, Sleep Duration, and Inflammation: A Systematic Review and Meta-Analysis of Cohort Studies and Experimental Sleep Deprivation. Biol Psychiatry. 2016 Jul 1;80(1):40-52.
- Fernandez-Mendoza, J., et al. (2021). Inflammation and Insomnia with Objective Short Sleep Duration. Sleep, 44(2).
- Kim, C. S., et al. (2023). Impact of psychological stress on gut microbiota and its implications for mental health. Gut Microbes, 15(1).
- Leerssen, J., et al. (2020). The fragmented sleep of insomnia: A systematic review and meta-analysis of sleep architecture. Sleep Medicine Reviews, 54.
- Xie, L., et al. (2023). Sleep drives metabolite clearance from the adult brain. Science.
- Fortier-Brochu, E., & Morin, C. M. (2021). Cognitive impairment in individuals with insomnia: Clinical significance and correlates. Sleep Medicine, 81.
- Lim, J., & Dinges, D. F. (2022). Sleep deprivation and vigilant attention. Annals of the New York Academy of Sciences, 1511(1).
- Wassing, R., et al. (2021). Restless REM Sleep Promotes the Overnight Growth of Emotional Reactivity. Current Biology, 31.
- Cryan, J. F., et al. (2022). The microbiota-gut-brain axis. Physiological Reviews, 99(4).
- O’Mahony, S. M., et al. (2021). Serotonin, tryptophan metabolism and the microbiota-gut-brain axis. Behavioural Brain Research, 411.
- Barrett, E., et al. (2020). γ-Aminobutyric acid production by cultured bacteria from the human intestine. Journal of Applied Microbiology, 129(6).
- Fulling, C., et al. (2021). Gut Microbes and the Vagus Nerve: In Search of a Golden Ticket. Trends in Neurosciences, 44(2).
- Diez-Gutiérrez, L., et al. (2020). Gamma-aminobutyric acid and probiotics: Multiple functions and starter culture potential in fermented foods. LWT – Food Science and Technology, 130.
- Silva, Y. P., et al. (2021). The Role of Short-Chain Fatty Acids From Gut Microbiota in Gut-Brain Communication. Frontiers in Endocrinology, 11.
- Del Toro-Barbosa, M., et al. (2021). Psychobiotics: Mechanisms of Action, Evaluation Methods and Effectiveness in Promoting Mental Health. Nutrients, 13(10).
- Vaiserman, A., et al. (2023). Gut microbiota and HPA axis: From bi-directional interactions to personalized medicine. Endocrine, 80.
- Nikolova, V. L., et al. (2023). Probiotics to treat depression: a systematic review and meta-analysis of randomized controlled trials. JAMA Psychiatry, 80(2).
- Smith, R. P., et al. (2023). Gut microbiome diversity is associated with sleep physiology in humans. PLoS ONE, 14(10).
- 台灣睡眠醫學學會 (2022). 台灣失眠盛行率與睡眠健康調查報告。
- 台灣益生菌協會 (2024). 精神益生菌臨床應用與安全性指引。
